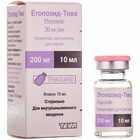
Этопозид-Тева
- Список товаров
- Цены в аптеках
- Аналоги
Нет в Днепре
Нет в Днепре
Инструкция указана для «Этопозид-Тева концентрат д/инф. 20 мг/мл по 10 мл (флакон)»
Действующее вещество: этопозид;
1 мл концентрата для раствора для инфузий содержит 20 мг этопозида;
Другие составляющие: кислота лимонная безводная, полисорбат 80, этанол безводный, полиэтиленгликоль.
Концентрат для раствора для инфузий.
Основные физико-химические свойства: прозрачный, слегка вязкий раствор желтоватого цвета практически без видимых частиц.
Антинеопластические средства. Производные подофилотоксина. Код ATX L01C B01.
Фармакодинамика
Этопозид является полусинтетическим производным подофилотоксина. Препарат нарушает синтез ДНК, ингибирует митоз, блокирует клетки преимущественно в G2-фазе и поздней S-фазе клеточного цикла. Цитотоксическое действие по отношению к здоровым клеткам отмечается только при применении высоких доз препарата.
Фармакокинетика
После введения фармакокинетика препарата двухфазовая с периодом полувыведения в первой фазе примерно 1,5 часа, во второй – 4-11 часов. Общий клиренс изменяется в пределах 33-48 мл/мин. Этопозид в незначительном количестве проникает в плевральную жидкость, определяется в слюне, печени, селезенке, почках, миометрии, в тканях мозга. В желчь поступает малое количество продукта. Этопозид плохо проникает через ГЭБ (концентрация этопозида в спинномозговой жидкости обычно варьирует от количества, не поддающегося определению, до менее чем 5% от концентрации в плазме крови в течение первых 24 часов после внутривенного введения). Этопозид в значительной степени (97%) связывается с белками плазмы крови.
Препарат метаболизируется в печени с образованием неактивной оксикислоты, а также глюкуронидов и сульфатов (5-22%), обладающих минимальной цитотоксической активностью. Выделяется преимущественно с мочой, в меньшем количестве (примерно 6%) – с желчью. У детей около 55% введенной дозы экскретируется с мочой в неизмененном состоянии в течение 24 часов. Средний почечный клиренс этопозида составляет 7-10 мл/мин или примерно 35% от общего клиренса при назначении препарата в дозе 80-600 мг/м 2 .
· Мелкоклеточная карцинома легких.
· Несеминомная карцинома яичка.
· Острый миеломоноцитарный и миелоцитарный лейкоз (ГМЛ, подтипы M4 или M5 по классификации FAB), в составе комбинированной терапии при неэффективности индукционной терапии.
· паллиативная терапия немелкоклеточного рака легких, реиндукционная терапия болезни Ходжкина, индукционная терапия неходжкинской лимфомы и острого миелоцитарного лейкоза, а также индукционная и реиндукционная терапия хориокарцином.
Повышенная чувствительность к этопозиду или другим компонентам препарата, выраженная миелосупрессия, тяжелые нарушения функции печени, тяжелые нарушения функции почек (клиренс креатинина (см. раздел «Применение в период беременности или кормления грудью»)).
При работе с препаратом необходимо соблюдать общие правила безопасности при обращении с потенциально токсичными веществами.
Следует избегать какого-либо контакта с этопозидом. При случайном попадании этопозида на кожу могут наблюдаться кожные реакции.
Медицинскому персоналу при работе с препаратом необходимо пользоваться защитной одеждой (перчатками, халатом), очками, маской. При попадании препарата в глаза или слизистые оболочки необходимо промыть их большим количеством проточной воды с мылом или 0,9% раствора натрия хлорида. Нельзя допускать к работе с препаратом беременных женщин.
Не обрабатывайте в автоклаве.
Этопозид нельзя использовать неразбавленным.
Срок хранения после разведения: 8 часов. Инфузия физически и химически стабильна до 120 часов при температуре 25 °C. Однако исходя из микробиологических особенностей рекомендуется готовить инфузию централизованно в фармацевтическом подразделении больниц и утилизировать ее в течение 8 часов.
После прокалывания резиновой пробки концентрат этопозида для инфузии остается стабильным в течение 72 часов (3 дня) при 25C. Поэтому он подходит для многократного использования.
Мутные растворы, а также растворы, содержащие осадок, непригодны для применения.
Взаимодействие с другими лекарственными средствами и другими видами взаимодействий
Совместное применение этопозида и циклоспорина в больших дозах может значительно увеличивать концентрацию этопозида в сыворотке крови, что приводит к повышению риска побочных реакций. Вероятно, такой эффект приводит к уменьшению клиренса и увеличению объема распределения этопозида, когда концентрации циклоспорина в сыворотке крови превышают 2000 нг/мл. Дозу этопозида при параллельном применении инфузий циклоспорина в высоких дозах необходимо снизить на 50%.
Комбинированная терапия с цисплатином связана с уменьшением общего клиренса этопозида.
Применение вместе с фенитоином, напротив, связано с увеличением общего клиренса этопозида и уменьшением его эффективности.
При одновременном применении с пероральными антикоагулянтами действие последних может усиливаться.
Сопутствующая терапия варфарином может привести к увеличению международного нормализованного соотношения (МЧС). Рекомендуется тщательное отслеживание протромбинового времени.
Вакцинация живыми вакцинами пациентов с ослабленным иммунитетом после химиотерапии может вызвать развитие тяжелых и летальных инфекций.
При применении этопозида в сочетании с другими цитотоксическими препаратами (в частности, метотрексатом и цисплатином) наблюдается синергический терапевтический эффект.
Фенилбутазон, натрия салицилата и салициловая кислота могут уменьшать связывание этопозида с белками плазмы крови.
Экспериментально было установлено наличие перекрестной резистентности между антрациклинами и этопозидом.
Этопозид может усиливать цитотоксическое и миелосупрессивное действие других препаратов.
Сообщалось о случаях острого лейкоза с предлейкозной фазой или без нее у пациентов, применяющих этопозид в сочетании с другими противоопухолевыми средствами, например блеомицином, цисплатином, ифосфамидом, метотрексатом.
Лечение Этопозидом-Тева может осуществлять только опытный врач-онколог в условиях специализированного стационара. При применении могут возникать реакции в месте инъекции.
Этопозид нельзя вводить внутриартериально, внутриплеврально и внутриперитонеально.
Этопозид предназначен только для внутривенного введения!
Во время внутривенного применения следует соблюдать осторожность во избежание экстравазации. Рекомендуется внимательно наблюдать место введения на предмет возможной инфильтрации во время применения препарата.
При возникновении экстравазации препарата следует немедленно прекратить и остаток раствора ввести в другую вену. При этом терапевтические мероприятия могут включать прикладывание холода, промывание изотоническим раствором хлорида натрия и местную инфильтрацию кортикостероидами. Пока неизвестно специфическое лечение реакций экстравазации.
Этопозид вводить путем медленной внутривенной инфузии в течение 30-60 минут, быстрое внутривенное введение может привести к артериальной гипотензии. Продолжительность инфузии этопозида зависит от индивидуальной реакции пациента и может удлиняться в случае необходимости. Выраженность снижения АД снижается при удлинении длительности инфузии.
Следует учитывать возможность развития анафилактических реакций с такими проявлениями как приливы (гиперемия), тахикардия, бронхоспазм и гипотензия (см. побочные реакции). При развитии анафилактических реакций необходимо немедленно прекратить инфузию препарата, назначить кортикостероиды, антигистаминные средства, коррекцию объема циркулирующей крови.
Этопозид следует с осторожностью назначать пациентам с сердечными аритмиями, инфарктом миокарда в анамнезе, нарушениями функции печени или почек, периферической нейропатией, нарушениями мочеиспускания, эпилепсией или повреждениями головного мозга, воспалением слизистой оболочки ротовой полости, а также больным.
У пациентов, лечащихся Этопозидом-Тева, необходимо тщательно контролировать угнетение функции костного мозга во время и после лечения. Может возникнуть тяжелая миелосупрессия с развитием инфекций или возникновением кровотечений. Были зарегистрированы случаи развития миелосупрессии с летальным исходом после введения препарата этопозид. Пациентов, проходящих терапию препаратом этопозид, необходимо регулярно и тщательно проверять наличие миелосупрессии как во время, так и после терапии.
Дозозависимое подавление функции костного мозга является наиболее распространенной формой токсического воздействия этопозида. В начале терапии этопозидом, а также перед каждым последующим введением следует проводить анализ состава периферической крови: количество тромбоцитов; гемоглобин; количество лейкоцитов; дифференциальный подсчет клеток крови
Если угнетение функции костного мозга развивается в результате лучевой терапии или химиотерапии, необходимо сделать перерыв.
Если количество лейкоцитов меньше 2000/мм 3 или количество тромбоцитов составляет 150000/мм 3 и менее, лечение следует прекратить до полной нормализации гематологических показателей (приблизительно через 10 дней).
Этопозид не рекомендуется применять пациентам с количеством нейтрофилов 3 (1,5×10 9 /л) или с количеством тромбоцитов 3 (100 × 10 9 /л), если это снижение не обусловлено злокачественным образованием.
Модификация дозирования после начальной дозы должна быть проведена, если количество нейтрофилов меньше 500/мм 3 (0,5 × 10 9 /л) в течение 5 и более дней или снижение связано с лихорадкой или инфекцией, если количество тромбоцитов меньше 25000 /мм 3 (25 × 10 9 /л), если возникают другие признаки токсичности степеней тяжести 3 или 4, а также если скорость почечного клиренса меньше 50 мл/мин. В случае депрессии костного мозга, развивающегося в результате лучевой терапии или химиотерапии, применение препарата следует приостановить. Рекомендуется не приступать к повторному лечению этопозидом до достижения количества тромбоцитов минимум 100000/мм 3 .
Развитие острой лейкемии, которая может сопровождаться миелодиспластическим синдромом, было зарегистрировано у пациентов, проходивших химиотерапию с применением этопозидсодержащих препаратов.
Кумулятивный риск или факторы, способствующие развитию вторичной лейкемии, пока неизвестны. Роль обеих схем лечения и накопления препарата этопозид были отмечены, но не описаны четко.
В некоторых случаях вторичной лейкемии у пациентов, проходивших терапию эпиподофилотоксинами, наблюдалась аномалия хромосомы 11q23. Эта аномалия также наблюдалась у пациентов с вторичной лейкемией после химиотерапии с применением схем лечения, не включавших препаратов-эпиподофилотоксинов, и с лейкемией, развивавшейся de novo . Другим фактором, связанным с вторичной лейкемией среди пациентов, проходивших терапию эпиподофилотоксинами, был короткий латентный период – медианное время для развития лейкемии было примерно 32 месяца.
Врачи должны учитывать возможное возникновение анафилактических реакций на препарат этопозид, симптомами которых являются озноб, лихорадка, тахикардия, остановка дыхания и снижение давления, которые могут привести к летальному исходу. Лечение является симптоматическим. Необходимо сразу прекратить инфузию препарата, ввести вазопрессорные препараты, кортикостероиды, антигистаминные препараты или плазмозаменители по выбору врача.
Во всех случаях, когда применение препарата этопозид выбрано для химиотерапии, врач должен оценить потребность и пользу препарата по сравнению с риском нежелательных реакций. Большинство таких реакций подвергаются коррекции, если их обнаружить вовремя. Если возникают тяжелые реакции, следует уменьшить дозу препарата или прекратить его прием, а также применить корректирующие меры в соответствии с клинической оценкой врача. Повторное назначение препарата следует проводить осторожно и с оценкой дальнейшей потребности в приеме препарата, а также с учетом возможного повторного возникновения токсичности.
Необходимо контролировать показатели периферической крови и функции печени.
Пациенты с низким уровнем сывороточного альбумина могут подвергаться повышенному риску токсичности этопозида. Пациенты с печеночной и почечной недостаточностью регулярно проводят диагностику функций указанных органов из-за риска накопления.
Бактериальные инфекции необходимо лечить до начала терапии этопозидом.
У пациентов с умеренными (клиренс креатинина от 15 до 50 мл/мин.) или тяжелыми (клиренс креатинина
Препарат содержит полисорбат 80. Сообщалось, что у недоношенных детей применение инъекционного витамина Е, также содержащего полисорбат 80, привело к таким опасным для жизни явления как синдром печеночной и почечной недостаточности, нарушение функций легких, тромбоцитопения и асцит.
Препарат содержит 24 об. % этанола. Каждая ампула содержит 5 мл до 1,2 г спирта, каждая 10 мл ампула содержит до 2,4 г спирта. Это может быть вредно для пациентов с заболеваниями печени, алкоголизмом, эпилепсией, мозговой травмой или заболеванием мозга. Спирт также может изменять или усиливать эффекты других лекарственных средств.
Вследствие отсутствия достаточных данных по применению этопозида в период беременности рекомендуется применять препарат только по жизненным показаниям.
Пациенткам репродуктивного возраста следует избегать наступления беременности. Если во время применения этопозида наступила беременность, женщина должна быть проинформирована о возможном риске для плода.
Поскольку этопозид может оказывать мутагенное действие, женщинам и мужчинам рекомендуется применять эффективную контрацепцию при лечении и в течение 6 месяцев после окончания терапии. Если после завершения терапии этопозидом пациентка желает иметь детей, рекомендуется провести генетическое тестирование.
Ввиду возможного влияния на фертильность пациентам-мужчинам рекомендуется прибегнуть к криоконсервации их спермы до начала терапии этопозидом.
До сих пор неизвестно, экскретируется ли этопозид в грудное молоко, поэтому нельзя исключить развитие нежелательных эффектов у кормящих грудью детей. Учитывая это, следует рассмотреть решение о прекращении применения препарата или отказ от кормления грудью в случае необходимости со стороны матери в применении этопозида.
Нет данных о влиянии этопозида на скорость реакции при управлении автотранспортом или работе с другими механизмами. Если существует риск развития побочных реакций со стороны ЦНС (сонливость, повышенная утомляемость) или транзиторная корковая слепота, следует избегать управления автотранспортом или работы с другими механизмами.
Препарат вводить только медленной внутривенной инфузии в течение 30-60 минут.
Доза этопозида-Тева составляет 60-120 мг/м 2 площади поверхности тела в сутки в течение 5 последовательных дней, повторные курсы с интервалом 10-20 дней. При лечении негематологических онкологических заболеваний интервалы между курсами должны быть не менее 21 дня. Содержимое флакона необходимо растворить непосредственно перед применением в 5% растворе глюкозы или 0,9% растворе натрия хлорида (100 мг этопозида на 500 мл). Всего проводить 3-4 курса лечения.
Повторные курсы химиотерапии проводить только после нормализации гематологических показателей.
Дозы и количество циклов лечения следует устанавливать также с учетом состояния костного мозга и ответной реакции опухоли на лечение.
Коррекция дозы
Дозировка препарата этопозид должна модифицироваться в соответствии с миелосупрессивными эффектами других препаратов в комбинации или результатами предварительной лучевой терапии или химиотерапии, что может уменьшать резерв костного мозга.
Начать новый курс терапии препаратом этопозид можно только в случае, если количество нейтрофилов не менее 1500/мм 3 (1,5 × 10 9 /л), а количество тромбоцитов не менее 100000/мм 3 (100 × 10 9 /л), кроме случаев снижения показателей, вызванных новообразованиями
Модификация дозирования после начальной дозы должна быть проведена, если количество нейтрофилов меньше 500/мм 3 (0,5 × 10 9 /л) в течение 5 и более дней, или снижение связано с лихорадкой или инфекцией, если количество тромбоцитов является менее 25000/мм 3 (25×10 9 /л), если возникают другие признаки токсичности степеней тяжести 3 или 4, а также если скорость почечного клиренса менее 50 мл/мин.
Пациенты пожилого возраста : корректировка дозы не требуется кроме основанной на функции почек.
Пациенты с нарушениями функции почек
Коррекция доз этопозида в зависимости от клиренса креатинина осуществляется в соответствии с приведенными ниже рекомендациями.
|
Клиренс креатинина |
Процент стандартной дозы Этопозида -Тева |
|
> 50 мл/мин |
100% |
|
15-50 мл/мин |
75 % |
Дальнейшая дозировка должна основываться на переносимости пациентом и клиническом эффекте. Пока нет данных по оптимальной дозировке в группе пациентов с уровнем клиренса креатинина
Пациенты с нарушением функции печени
Сообщалось, что гематологическая токсичность, вызванная этопозидом, была более серьезной у пациентов с повышенными концентрациями билирубина в сыворотке крови. Также известно, что общий плазменный клиренс и элиминация этопозида могут быть снижены у пациентов с ухудшающейся печеночной функцией. Поэтому таким пациентам это следует применять с осторожностью и принимать во внимание возможную необходимость уменьшения дозы.
Дети. Препарат не использовать детям.
Острая передозировка сопровождается тяжелыми проявлениями побочных реакций, особенно лейкопенией и тромбоцитопенией.
Внутривенное введение этопозида в общей дозе 2,4-3,5 г/м 2 поверхности тела в течение трех дней привело к тяжелому мукозиту и угнетению функции костного мозга. Сообщалось о тяжелых гепатотоксических эффектах и развитии метаболического ацидоза у пациентов, получавших этопозид в дозах выше рекомендованных. Специфический антидот этопозида неизвестен. При передозировке назначают симптоматическое и поддерживающее лечение, включая переливание эритроцитарной и/или тромбоцитарной массы и антибиотикотерапию. При гиперчувствительности к препарату следует назначать антигистаминные препараты и введение кортикостероидов.
Доброкачественные и злокачественные новообразования (включая кисты и полипы): вторичный острый лейкоз (с предлейкозной фазой или без нее) у пациентов, лечившихся этопозидом в сочетании с другими антинеопластическими препаратами.
Инфекции и инвазии: лихорадка, сепсис.
Со стороны системы крови и лимфатической системы: миелосупрессия (и с летальным исходом), лейкопения, тромбоцитопения, снижение уровня гемоглобина, кровотечения вследствие тяжелой миелосупрессии, анемия, нейтропения.
Со стороны сердечно-сосудистой системы: инфаркт миокарда, аритмия, боли в области сердца, транзиторная артериальная гипотензия (при очень быстром введении препарата), артериальная гипертензия, (артериальное давление обычно нормализуется в течение нескольких часов после завершения введения препарата), приливы, ф. отек.
Со стороны иммунной системы: анафилактические реакции (могут иметь летальные исходы) с такими проявлениями как озноб, приливы, тахикардия, одышка, бронхоспазм, артериальная гипотензия.
Со стороны нервной системы: периферическая нейропатия, боли в пояснице, судороги (иногда связанные с аллергическими реакциями), спутанность сознания, гиперкинезия, акинезия, головокружение, нейротоксичность (в т. ч. сонливость, повышенная утомляемость), изменения вкуса, транзитор слепота.
Со стороны органов зрения: неврит зрительного нерва, слезотечение.
Со стороны дыхательной системы, органов грудной клетки и средостения: апноэ со спонтанным восстановлением дыхания после окончания лечения этопозидом, внезапные летальные реакции, связанные с бронхоспазмом, кашель, ларингоспазм, цианоз, интерстициальный пневмонит/легочный фиброз; насморк, пневмония.
Со стороны желудочно-кишечного тракта: тошнота, рвота, диарея, анорексия, мукозит (в т. ч. стоматит и эзофагит), боль в животе, запор, дисфагия, дисгевзия.
Со стороны гепатобилиарной системы: гепатотоксичность, повышение уровня печеночных ферментов, повышение уровня мочевины и креатинина, повышение уровня билирубина.
Метаболические и алиментарные нарушения: гиперурикемия, метаболический ацидоз.
Со стороны кожи и подкожных тканей: обратимая алопеция (иногда полное выпадение волос), отек лица и языка, усиленное потоотделение, сыпь, крапивница, изменения пигментации кожи, зуд, дерматит, возврат симптомов лучевого дерматита, токсический эпидермальный некролиз, синдром. Джонсон, ладонно-подошвенный синдром.
Со стороны почек и мочевыводящей системы: поскольку в почках достигаются высокие концентрации этопозида, он может нарушать функцию почек вследствие кумуляции.
Со стороны репродуктивной системы и молочных желез: аменорея, ановуляторные циклы, понижение фертильности, гипоменорея, азооспермия.
Общие нарушения и местные реакции: астения, недомогание, экстравазация (в т. ч. реакции со стороны мягких тканей: отек, боль, целлюлит, некроз, включая некроз кожи), повышенная утомляемость, флебит.
Описание отдельных побочных реакций
Гематологическая токсичность.
Сообщалось о миелосупрессии с летальным исходом после введения этопозида. Миелосупрессия часто носила дозозависимый характер. Обычно восстановление костного мозга происходило на 20-й день и не наблюдалась кумулятивная токсичность. Самый низкий уровень гранулоцитов и тромбоцитов обычно наблюдался через 10-14 дней после приема препарата в зависимости от способа введения и схемы лечения. Самый низкий уровень достигается быстрее внутривенного введения, по сравнению с пероральным.
Среди пациентов с нейтропенией, проходивших терапию препаратом этопозид, также часто возникали лихорадка и инфекционные заболевания.
Желудочно-кишечная токсичность.
Тошнота и рвота были наиболее распространенными проявлениями желудочно-кишечной токсичности препарата этопозид. Обычно эти симптомы корректировались антиэметические препараты. Также наблюдалась диарея.
Алопеция.
Оборотная алопеция, часто приводящая к полному полисению, наблюдалась у многих пациентов, проходивших терапию препаратом этопозид.
Артериальная гипотензия.
Сообщалось о неустойчивой артериальной гипотензии, возникавшей после быстрого введения этипозида, которая не была связана с изменениями в электрокардиограмме или кардиологической токсичностью. Гипотензия часто является ответом на прекращение инфузии этопозида и/или другой поддерживающей терапии. При продолжении инфузии рекомендуется замедлить введение. Не было зарегистрировано случаев гипотензии, отложенных во времени.
Артериальная гипертензия.
При терапии этопозидом сообщалось о возникновении гипертензии. Если возникает клинически значимая гипертензия, необходимо приступить к соответствующей поддерживающей терапии.
Аллергические реакции.
Также сообщалось о реакциях анафилактического типа во время или сразу после внутривенного введения препарата этопозид. Пока не определена роль, которую играет концентрация или скорость инфузии в развитии реакции анафилактического типа. Обычно давление нормализуется в течение нескольких часов после окончания инфузии. Реакция анафилактического типа может возникать после первой дозы препарата.
Также сообщалось о случаях острой реакции с бронхоспазмом, которые привели к летальному исходу.
Метаболические осложнения
Сообщалось о синдроме лизиса опухоли (иногда фатального) после использования этопозида в сочетании с другими химиотерапевтическими препаратами. Для выявления ранних признаков синдрома лизиса опухоли необходим тщательный мониторинг пациентов, особенно у пациентов с такими факторами риска, как массивные чувствительные к лечению опухоли и почечная недостаточность. Соответствующие профилактические меры следует учитывать у пациентов с риском этого осложнения терапии.
3 года.
Хранить в оригинальной упаковке при температуре не выше 25 ºС в защищенном от света и недоступном для детей месте.
Раствор Этопозида-Тева нельзя смешивать в одном объеме с другими препаратами для парентерального введения, кроме растворителей, указанных в разделе «Способ применения и дозы».
Этопозид-Тева фармацевтически несовместим с растворами, имеющими щелочные значения рН.
Сообщалось о растрескивании деталей шприцев и инфузионных систем, изготовленных из акриловых полимеров или акрилнитрил-бутадиен-стирола (АБС), при контакте с неразбавленным концентратом для инфузий Этопозид-Тева 20 мг/мл. С разбавленными растворами для инфузий этот эффект не наблюдается.
По 5 или 10 мл во флаконе, покрытом защитным покрытием TevaGuard; по 1 флакону в коробке.
По рецепту.
Фармахеми Б. В.
Адрес
Ул. Свенсвег 5, 2031 GA Харлем, Нидерланды.

Нет в Днепре

Нет в Днепре