Блицеф
- Список товаров
- Цены в аптеках
- Аналоги
Товаров: 1
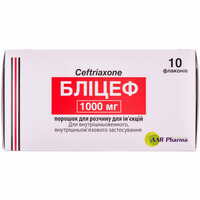
Зейсс Фармасьютикелс (Индия)
Блицеф
от 1065.45 ₴
По рецепту
в 5 аптеках
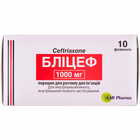
Инструкция для Блицеф порошок д/ин. по 1000 мг №10 (флаконы)
Инструкция указана для «Блицеф порошок д/ин. по 1000 мг №10 (флаконы)»
Цена на Блицеф начинается от 1065.45
| Название | Цена ₴ |
|---|---|
| Блицеф порошок д/ин. по 1000 мг №10 (флаконы) | 1065.45 ₴ |
Аналоги

от 47.80 ₴
в 153 аптеках
от 203.98 ₴
в 2 аптеках

от 202.49 ₴
в 141 аптеке

от 167.85 ₴
в 113 аптеках
Нспс Хебей Хуамин Фармасьютикал Компани (Китай)
от 476.65 ₴
в 31 аптеке
от 234.30 ₴
в 6 аптеках

от 173.56 ₴
в 46 аптеках

от 38.17 ₴
в 2 аптеках
от 33.70 ₴
в 33 аптеках

от 188.20 ₴
в 126 аптеках
от 277.32 ₴
в 5 аптеках

от 41.03 ₴
в 123 аптеках
от 27.21 ₴
в 4 аптеках

от 188.36 ₴
в 2 аптеках
от 165.10 ₴
в 3 аптеках

Свисс Перентералс (Индия)
Нет в Одессе
от 569.00 ₴
в 154 аптеках

от 429.20 ₴
в 146 аптеках

от 887.30 ₴
в 36 аптеках

от 945.52 ₴
в 5 аптеках
от 35.80 ₴
в 34 аптеках

от 173.43 ₴
в 7 аптеках

от 2535.34 ₴
в 3 аптеках

от 423.50 ₴
в 24 аптеках
Нет в Одессе

от 140.20 ₴
в 130 аптеках

Юрия Фарм (Украина)
от 550.56 ₴
в 3 аптеках
от 70.40 ₴
в 1 аптеке

от 501.60 ₴
в 24 аптеках

Нет в Одессе

Киевмедпрепарат (Украина)
от 271.99 ₴
в 61 аптеке

Нет в Одессе

от 40.85 ₴
в 2 аптеках

Нспс Хебей Хуамин Фармасьютикал Компани (Китай)
от 56.25 ₴
в 3 аптеках

от 56.50 ₴
в 33 аптеках
Нет в Одессе

от 1494.40 ₴
в 34 аптеках
Также ищут
Искать в других городах
Беляевка
Винница
Днепр
Доброслав
Житомир
Запорожье
Измаил
Киев
Коблево
Кременчуг
Кривое Озеро
Кривой Рог
Кропивницкий
Львов
Николаев
Полтава
Помошная
Снигиревка
Сумы
Татарбунары
Харьков
Хлебодарское
Черкассы
Чернигов
Южноукраинск
Другие изображения Блицеф
Просмотренные товары

Техномедика (Украина)
Medtextile 1005
от 530.10 ₴

Мир Пожилого Человека (Украина)
Medok


Укрмедтекстиль (Украина)
Пакет

Фарммедальянс (Украина)
Фарммедальянс
Выберите товар
Выберите товар