Фулвестрант-Виста
- Список товаров
- Цены в аптеках
- Аналоги
Товаров: 1
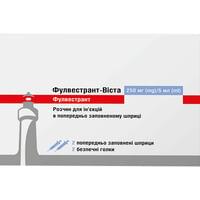
Лабораториос Фармалан (Испания)
Фулвестрант-Виста
Нет в Херсоне
По рецепту
Цены в
Инструкция для Фулвестрант раствор д/ин. 250 мг / 5 мл по 5 мл №2 (шприцы)
Инструкция указана для «Фулвестрант раствор д/ин. 250 мг / 5 мл по 5 мл №2 (шприцы)»
Аналоги

Астра Зенека (Великобритания)
Нет в Херсоне
Также ищут
Искать в других городах
Другие изображения Фулвестрант-Виста

Просмотренные товары





Выберите товар
Выберите товар





